saiba mais
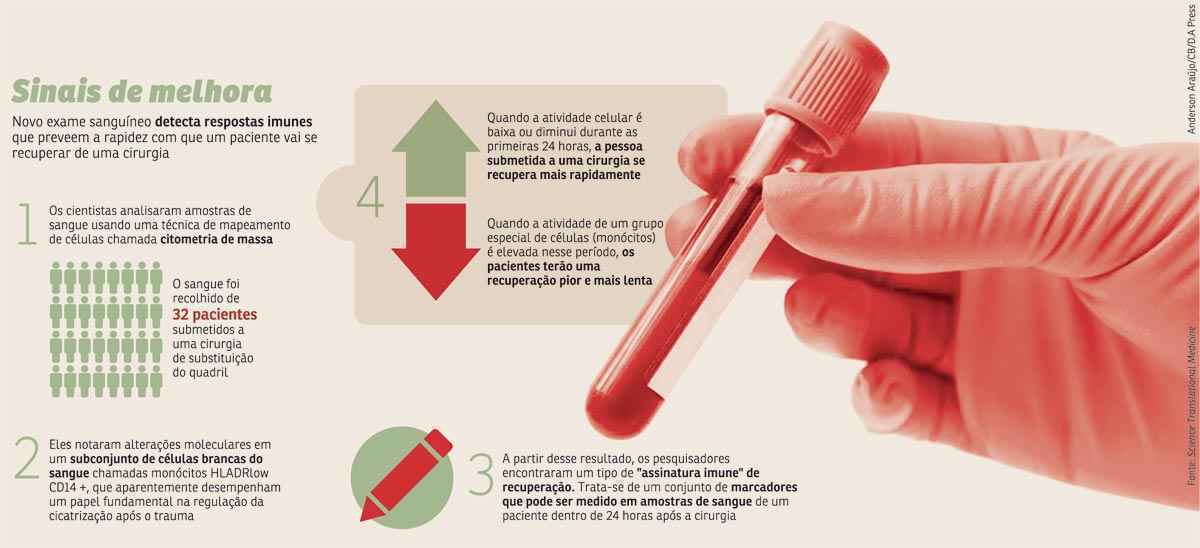
Pesquisadores da Universidade de Stanford, nos Estados Unidos, usaram um exame já conhecido, a citometria de massa, para caracterizar danos imunológicos pós-cirúrgicos em um nível meticuloso: uma única célula. Eles encontraram um tipo de assinatura imunológica cirúrgica que se correlaciona com a recuperação clínica de pacientes. As pistas para formar essa assinatura vieram de amostras sanguíneas de 32 pessoas submetidas a uma cirurgia de substituição do quadril.
O mapeamento detalhado mostrou que respostas na forma de sinalização celular — e não na frequência de células — foram relacionadas à recuperação. Essas reações de sinalização correlacionadas ao pós-operatório ocorreram sobretudo em monócitos CD14 +, um tipo de célula de defesa. O resultado sugere que essas estruturas podem desempenhar papel predominante na recuperação cirúrgica.
Dessa forma, quando a atividade nesse grupo é elevada nas primeiras 24 horas após a cirurgia, os pacientes têm uma recuperação pior. Se a atividade celular é baixa, as pessoas respondem melhor. “A consistência dessa assinatura sugere uma resposta imune bem regulamentada ao trauma cirúrgico que, se validada, pode formar a base de uma diretriz de diagnóstico para o cuidado pós-cirúrgico personalizado”, afirma o principal autor da pesquisa, Brice Gaudillière.
Os cientistas cogitam ainda que os resultados possam levar ao desenvolvimento de um teste pré-operatório para ajudar médicos a determinar não só o tempo de recuperação da cirurgia, mas também identificar pacientes para os quais os riscos do procedimento superam os benefícios. Mário Sérgio Fernandes, professor de hematologia do Hospital São Lucas da Faculdade de Medicina da Pontifícia Universidade Católica do Rio Grande do Sul, pondera que uma aplicação clínica do exame ainda está muito distante.
“A proposta é inicial, mas muito interessante. Os resultados são promissores, mas não deixaram claro o que pode diferenciar os pacientes somente olhando para as atividades moleculares que foram mostradas”, justifica. Fernandes também ressalta que o teste proposto pelos estudiosos de Stanford é normalmente usado em investigações científicas em casos de leucemias e neoplasias. “O equipamento utilizado para esse exame é encontrado normalmente em grandes hospitais.”
Fatores múltiplos
Depois da cirurgia, o organismo humano costuma seguir uma resposta padrão. O primeiro movimento, chamado catabolismo, consiste em tentar dar o máximo possível de glicose e oxigênio em busca de um reforço na reabilitação. O segundo, anabolismo, tenta recuperar o que foi perdido. Em ambas as fases, proteínas são retiradas da musculatura, gorduras deixam os reservatórios e o fígado e tudo é jogado dentro do sangue para conseguir que a pessoa tenha uma recuperação normal.
“Há ainda a ação dos hormônios dentro do organismo, como o que diminui a urina do paciente”, complementa Sérgio Arap, gerente médico do Centro Cirúrgico do Hospital Sírio-Libanês. Por esse motivo, é comum a sensação de inchaço após o procedimento. O corpo, na verdade, tenta acumular o máximo possível de líquido para se recuperar. Arap alerta, no entanto, que todos esses fatores variam muito conforme o tamanho da cirurgia, do trauma e o paciente.
Ser diabético, hipertenso, atleta e ter problemas renais são, segundo o especialista, condições que interferem no resultado final do procedimento médico. “Quando colocamos todos (tipos de pacientes) juntos, também identificamos que, às vezes, um é internado um dia só e outro que fez uma cirurgia igualzinha fica quatro, cinco dias. A resposta metabólica é diferente e, se houver algum exame que possa predizer isso, será interessante ter esses dados antes da cirurgia.”

Metodologia promissora
“A citometria de massa é uma tecnologia muito recente e difere da citometria de fluxo tradicional. Tem a capacidade de avaliar simultaneamente cerca de 50 parâmetros celulares diferentes, revelando perfis imunofenotípicos associados a cânceres, inflamações, infecções, entre outros padrões de resposta biológica. As proteínas humanas são pesquisadas utilizando anticorpos associados a metais pesados da tabela periódica. A amostra, ao ser introduzida no equipamento, é atomizada, ionizada e pulverizada sob altas temperaturas, gerando nuvens de carbono e hidrogênio com massa e carga características de componentes celulares específicos. Essa metodologia está disponível apenas no campo da pesquisa, mas é altamente promissora em cenários clínicos, uma vez que pode avaliar a integridade ou não de sistemas proteicos que garantem funções biológicas como morte e vida da célula, reparos no DNA e resposta imunológica. Além disso, a metodologia tem potencial para identificar moléculas anômalas possibilitando o uso de medicamentos altamente específicos contra esses alvos celulares indesejáveis.”
Mirtes Sales, membro da Sociedade Brasileira de Patologia Clínica e responsável pelo Laboratório de Citometria de Fluxo do Hospital das Clínicas da Faculdade de Medicina da Universidade de São Paulo