Os resultados de dois estudos que usaram o método da terapia gênica foram publicados na edição desta semana da revista Science. Com vírus da família do HIV geneticamente modificados, os pesquisadores conseguiram consertar mutações dentro das células, uma possibilidade levantada ainda em 1996 também por cientistas da Itália. Foram mais de 15 anos de testes frustrados em laboratório até que a ideia se mostrasse possível. “Esse tipo de tratamento sempre era um sucesso nos modelos animais (ratos) usados nas pesquisas, mas em humanos isso não acontecia, o que impossibilitava a aplicação clínica”, conta Alessandro Aiutti, coordenador de um dos estudos e chefe do Departamento de Pesquisas Clínicas Pediátricas para Terapia Gênica do Instituto Telethon San Raffaele, em Milão.
saiba mais
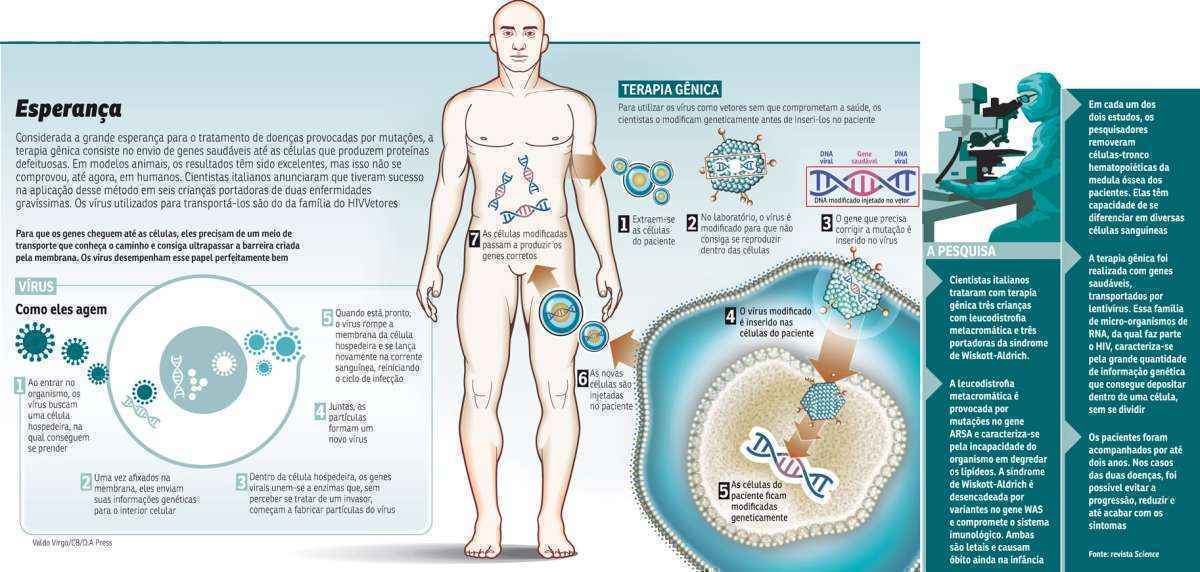
A leucodistrofia é um distúrbio metabólico: por causa de mutações no gene ARSA, o organismo não consegue quebrar as moléculas de gordura. “Mesmo se o paciente não comer nada gorduroso, os lipídios produzido pelo próprio corpo vão se acumulando, o que desencadeia uma série de sintomas gravíssimos. A maioria dos pacientes morre aos 5 anos, em média, e não há tratamento específico para essa doença”, conta Alessandra Biffi, pesquisadora da Divisão de Células-Tronco do Instituto Telethon San Raffaele e principal autora de um dos artigos publicados na Science. O mal começa a se manifestar entre os 12 e 20 meses de vida, caracterizando-se por falta de controle muscular e motor, além de deficit de reflexos. Segundo um estudo da Universidade do Texas, a incidência da leucodistrofia metacromática varia bastante, podendo atingir um em cada 40 mil ou 160 mil pessoas.
Enquanto essa enfermidade atinge ambos os sexos, a síndrome de Wiskott-Aldrich afeta apenas meninos. Devido a mutações no gene WAS, o sistema imunológico torna-se muito mais vulnerável ao desenvolvimento de infecções, doenças autoimunes, câncer e deficiência plaquetária, o que causa sangramentos frequentes. Em média, os pequenos pacientes vivem até os 10 anos e, quando ultrapassam essa expectativa, desenvolvem leucemias e outros cânceres de sangue. “O portador do distúrbio pode até ser curado em alguns casos, mas, para isso, precisa de um transplante de medula óssea. Nem sempre, porém, é possível encontrar um doador que seja 100% compatível”, explica Jordan Orange, professor de imunologia pediátrica da Universidade do Texas que colaborou com o estudo italiano. “Para essas crianças, que não encontram doadores, é que a pesquisa foi desenhada”, diz.
Vetores
Uma das dificuldades da terapia gênica é levar para dentro das células as informações necessárias para a produção de proteínas saudáveis, no lugar dos genes deficientes. No campo da oftalmologia, os adenovírus estão desempenhando muito bem a tarefa de romper a barreira formada pela membrana, mas esses micro-organismos não conseguem inserir a quantidade suficiente de material para consertar as mutações que se manifestam em alguns tipos de célula. Testes realizados com retrovírus mostraram que, enquanto esses atingem o objetivo, também acabam provocando a formação de tumores malignos. Já os lenivírus, além de transferirem bastante informação genética para o núcleo celular, não causam cânceres. Por isso, foram escolhidos para os estudos italianos.
Antes de usá-los como meio de transporte, foi preciso, em primeiro lugar, manipular os micro-organismos no laboratório para retirar deles o potencial infeccioso. Com reengenharia, os cientistas conseguiram produzir vetores que chegam ao local certo, levam os genes saudáveis e não fazem mal à saúde. Depois, eles retiraram da medula óssea dos pacientes células-tronco hematopoiéticas, as precursoras de todas as células sanguíneas, como leucócitos, hemáceas e plaquetas. No laboratório, elas foram colocadas com os vírus para que esses rompessem a membrana e inserissem os genes corretos. Todo o material foi injetado de volta na corrente sanguínea dos pacientes.
Uma vez dentro das células, a produção das proteínas se normalizou. No caso da síndrome de Wiskott-Aldrich, sintomas como infecções recorrentes e eczema retrocederam. Já os três pacientes de leucodistrofia metacromática foram tratados ainda bebês, antes que os sinais da doença se manifestassem. Passados três anos de testes, eles continuavam sem apresentar as características da enfermidade. “Os resultados obtidos com os seis primeiros pacientes são muito encorajantes: a terapia não é apenas segura, mas também efetiva e capaz de mudar a história clínica dessas doenças severas. Foram 15 anos de esforços, frustrações e sucesso no laboratório; então, agora é realmente maravilhoso conseguirmos oferecer uma solução concreta para os primeiros pacientes”, disse, em nota, Luigi Naldini, que dirigiu os dois estudos. Foi ele que, em 1996, levantou a hipótese de que vírus da família do HIV poderiam ser vetores para tratamento de doenças genéticas.
O geneticista Alessandro Aiutti explica que, nas crianças com síndrome de Wiskott-Aldrich, como as células do sangue são diretamente afetadas pela doença, a terapia corrigiu o problema in loco, normalizando a produção das plaquetas e dos linfócitos, que fazem o papel de defesa. “Graças à terapia gênica, as crianças não precisam mais enfrentar hemorragias e infecções, podendo brincar e correr e ir para a escola como todas as outras”, afirma. Já no caso da leucodistrofia metacromática, por ser uma enfermidade neurológica, o tratamento foi mais sofisticado. Como são estruturas do sangue, as células-tronco hematopoiéticas corrigidas viajaram da corrente sanguínea até o cérebro, onde liberaram os genes corretos. A quantidade de proteínas saudáveis superou as defeituosas, evitando o processo neurodegenerativo.
Agora, os pesquisadores precisam esperar mais tempo até que a terapia gênica com os lentivírus se mostre totalmente segura, abrindo caminho para a oferta em larga escala e beneficiando outros pacientes, além daqueles que participaram dos testes clínicos. Para eles, os dois estudos indicaram que esse método poderá ser útil para diversas outras doenças genéticas.