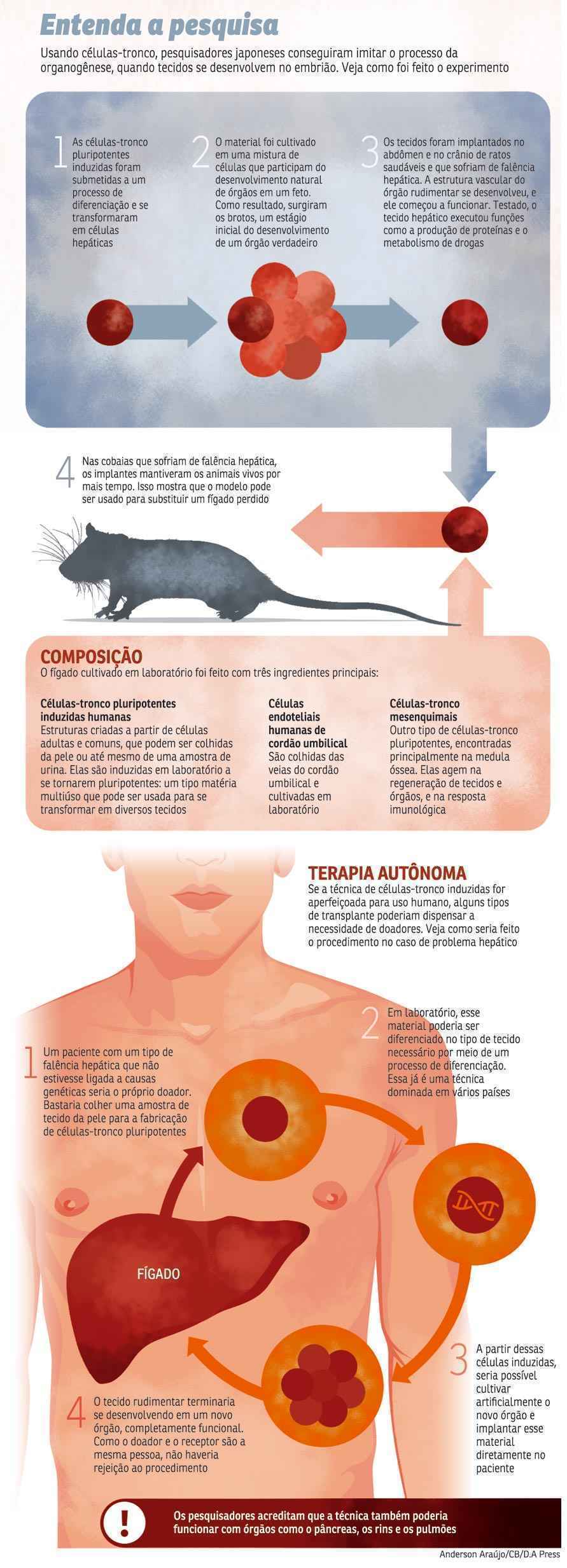
Até então, a criação de órgãos vascularizados era um desafio para a comunidade científica, que tentava manipular células-tronco para a geração desses tecidos complexos in vitro. O grande trunfo da equipe da Escola de Medicina da Universidade de Yokohama, no Japão, foi imitar em laboratório o ambiente natural de desenvolvimento de um feto. “O broto do fígado é formado no primeiro estágio de desenvolvimento. Normalmente em humanos, talvez por volta da quinta ou da sexta semana de gestação. Então, no estágio embrionário, o broto do fígado é formado in vivo. Nós basicamente imitamos esse processo de transição primitivo”, explica Takanori Takebe, principal autor do trabalho, publicado na revista Nature de hoje.
saiba mais
-
Pesquisadores criam guia para tratamento de pacientes que fizeram transplante de fígado
-
Fígado pode ser desintoxicado com alimentos específicos
-
Pesquisa da UFMG tenta evitar falência do fígado
-
Mutação ligada ao câncer de fígado é identificada no Brasil
-
Cientistas convertem células comuns em células-tronco
-
Brasileiros desvendam regeneração celular e descoberta chama atenção da comunidade científica mundial
O resultado foi uma série de fragmentos tridimensionais de 5 milímetros de tecido hepático, que foram implantados em ratos de laboratório e desenvolveram um sistema vascular próprio. Os enxertos de órgãos foram testados em laboratório e mostraram ter as mesmas funções de um fígado humano desenvolvido, como o metabolismo de drogas específicas e a produção de proteínas. Para isso, o fígado rudimentar foi colocado no crânio das cobaias, em que a observação das funções das células é feita com mais facilidade.
“Estamos agora planejando transplantar (diretamente) no fígado. Para fazer isso, temos de reduzir o tamanho dos brotos em pedaços muito pequenos, e, depois disso, tentaremos reprimir o fígado em 30% com tecido hepático de células iPS humanas”, adianta Takebe. Depois que conseguirem iniciar a produção em massa de brotos em tamanho micrométrico, dezenas de milhares de fragmentos de fígado poderiam ser injetados diretamente na corrente sanguínea das cobaias.
Os fragmentos também foram inseridos no abdômen de ratos que sofriam de falência hepática e melhoraram a saúde dos bichos. Isso significa que a técnica pode ser uma esperança para pacientes que precisam de um novo órgão. Além do fígado, os pesquisadores acreditam que o método possa ser replicado em células de órgãos como os rins e os pulmões, e já trabalham na criação de um pâncreas com a mesma técnica.
Otimismo
Para especialistas, esse experimento inédito pode ser um passo fundamental para a tão almejada produção de órgãos inteiros em laboratório a partir de células-tronco. “Já se sabia da possibilidade de usar uma célula pluripotente para dar origem a tipos celulares específicos in vitro, como numa placa de cultura. Esse trabalho demonstra a possibilidade de gerar um órgão funcional dentro de um organismo, no caso um camundongo”, anima-se Stevens Rehen, pesquisador do Laboratório Nacional de Células-Tronco Embrionárias do Instituto de Ciências Biomédicas da Universidade Federal do Rio de Janeiro (UFRJ).
O feito é uma prova do rápido desenvolvimento das pesquisas com células-tronco desde que elas começaram a ser usadas em experimentos com animais, em 1981. Foram necessários 17 anos para que pesquisas desse tipo passassem a usar tecidos humanos, e mais nove para o desenvolvimento da técnica que produziria as estruturas pluripotentes em laboratório, as iPS. Desde então, as pesquisas sofreram um acelerado avanço, impulsionado pela dispensa das controversas células embrionárias. Embora os tratamentos com o material ainda sejam relativamente raros, experimentos já testam o uso das iPS para a cura de diversas doenças de degeneração celular, como a paralisia e a cegueira.
Mas o maior objetivo dos pesquisadores sempre foi usar as células, embrionárias ou induzidas, para a fabricação de órgãos completos. “Eu estou muito otimista. Não há nenhum outro (experimento) que tenha avançado desde os primeiros indícios de uma funcionalidade de aplicação em um laboratório para uma aplicação in vivo”, aponta Stevens. Caso a técnica seja aperfeiçoada, seria possível gerar um novo fígado ou rim a partir do material genético do próprio paciente. O procedimento, além de dispensar a fila de espera por doadores, eliminaria a possibilidade de rejeição do tecido pelo organismo.
Cautela
No entanto, tanto pesquisadores quanto especialistas ressaltam que esse é apenas o primeiro passo de anos de pesquisa. Seriam necessários mais cinco anos para a produção em massa desses brotos de órgãos criados pelos japoneses, e outros cinco para o início dos testes em humanos. “É o início do entendimento. Não estamos dizendo que construíram totalmente um órgão, mas é uma pesquisa fantástica para começar esse tipo de desenvolvimento”, avalia Patricia Pranke, chefe do Laboratório de Hematologia e Células-Tronco da Universidade Federal do Rio Grande do Sul (UFRGS). O sucesso da experiência, ressalta a especialista, deve-se em parte à grande capacidade de regeneração do fígado, um objeto ideal para esse tipo de estudo.
Patrícia aponta que, tanto com o tecido hepático quanto com outros tipos de órgãos, a criação de uma estrutura completa como a desenvolvida em um corpo humano comum ainda depende da compreensão detalhada da formação de cada tipo de célula que compõe os diferentes tecidos, além da dominação da arte de replicar o delicado processo em laboratório. “A gente ainda não sabe qual é a forma correta de formar um órgão inteiro, é algo muito complexo. Tem vários tipos celulares envolvidos, desde a artéria, os vasos, o sangue. E construir o arcabouço tridimensional é um complicador”, exemplifica a pesquisadora brasileira.

Volta ao primitivo
“As células pluripotentes induzidas (iPS) são feitas a partir de uma célula somática, isto é, que não é sexual. Pega-se uma que tenha o código genético completo nos órgãos ou nos tecidos. O segredo é justamente conseguir fazer com que ela volte a um estágio bem primitivo. Teoricamente, o blastocisto, quando implantado no útero, vai formar um ser humano. Então, é óbvio que a célula embrionária sabe o caminho de gerar qualquer tecido do corpo, por isso ela é extremamente pluripotente. Só que as iPS vieram de uma célula somática, não embrionária, apesar de serem induzidas a se tornar pluripotentes. É como se gente pegasse uma célula somática e a fizesse virar um embrião. Manipulamos a estrutura geneticamente, ativando genes que fazem esse retrocesso, digamos assim. Então, essa célula começa a se comportar como se fosse uma célula-tronco embrionária. A vantagem é exatamente essa: você não trabalha com embrião, que tem questões éticas e religiosas. Mas a desvantagem é que é uma célula muito manipulada. O quanto poderemos usar na prática, a gente não sabe. Não é um processo natural, estamos mexendo muito na genética da célula.”
Patricia Pranke, chefe do Laboratório de Hematologia e Células-Tronco da Universidade
Federal do Rio Grande do Sul (UFRGS)